Physique-Chimie > Chimie Organique > Réactions en Chimie Organique (Notions) > Réactions de substitution, d'addition, d'élimination
Réactions Clés en Chimie Organique : Substitution, Addition et Élimination
Explorez les trois types de réactions fondamentales en chimie organique : substitution, addition et élimination. Comprenez leurs mécanismes, leurs conditions de réaction et leurs applications avec des exemples clairs et précis, adaptés au niveau lycée.
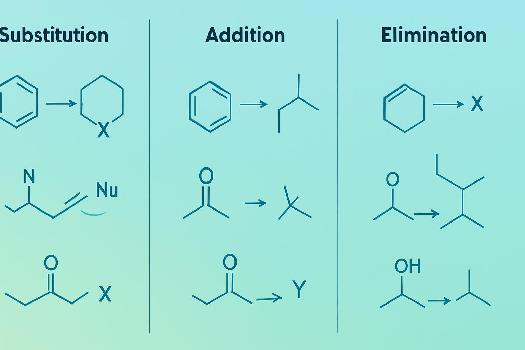
Introduction aux Réactions en Chimie Organique
En chimie organique, les réactions chimiques transforment des molécules en de nouvelles substances. Trois types de réactions sont particulièrement importants : les réactions de substitution, d'addition et d'élimination. Comprendre ces réactions est essentiel pour prédire et manipuler la synthèse de composés organiques.
Réactions de Substitution
Les réactions de substitution impliquent le remplacement d'un atome ou d'un groupe d'atomes (le groupe partant) par un autre atome ou groupe d'atomes (le nucléophile ou l'électrophile). Il existe deux principaux types de mécanismes de substitution :
- SN1 (Substitution Nucléophile Unimoléculaire): Cette réaction se déroule en deux étapes. La première étape est la formation d'un carbocation (ion chargé positivement). La deuxième étape est l'attaque du carbocation par le nucléophile. Les réactions SN1 sont favorisées par les solvants polaires protiques et les carbocations stables (tertiaires > secondaires > primaires).
- SN2 (Substitution Nucléophile Bimoléculaire): Cette réaction se déroule en une seule étape. Le nucléophile attaque simultanément l'atome de carbone tout en éjectant le groupe partant. La réaction SN2 se fait avec inversion de configuration (inversion de Walden). Elle est favorisée par les nucléophiles forts et les atomes de carbone peu encombrés (primaires > secondaires > tertiaires).
Réactions d'Addition
Les réactions d'addition impliquent l'ajout d'atomes ou de groupes d'atomes à une molécule, généralement à travers une liaison multiple (double ou triple liaison). Ce type de réaction convertit une liaison π en deux liaisons σ.
- Addition Électrophile: L'addition électrophile est fréquente sur les alcènes et les alcynes. L'électrophile (une espèce chimique qui cherche des électrons) attaque la liaison π riche en électrons. Par exemple, l'addition de bromure d'hydrogène (HBr) à l'éthène (CH2=CH2) forme du bromoéthane (CH3-CH2Br).
- Addition Nucléophile: L'addition nucléophile est fréquente sur les composés carbonylés (aldéhydes et cétones). Le nucléophile attaque le carbone du groupe carbonyle, qui est partiellement positif. Par exemple, l'addition de cyanure d'hydrogène (HCN) à l'éthanal (CH3CHO) forme une cyanohydrine.
Réactions d'Élimination
Les réactions d'élimination impliquent le retrait d'atomes ou de groupes d'atomes d'une molécule, conduisant à la formation d'une liaison multiple (double ou triple liaison). C'est l'inverse d'une réaction d'addition.
- E1 (Élimination Unimoléculaire): Cette réaction se déroule en deux étapes. La première étape est la formation d'un carbocation. La deuxième étape est l'abstraction d'un proton par une base, ce qui conduit à la formation d'un alcène. Les réactions E1 sont favorisées par les solvants polaires protiques et les carbocations stables.
- E2 (Élimination Bimoléculaire): Cette réaction se déroule en une seule étape. Une base forte arrache un proton, simultanément au départ du groupe partant, formant une liaison π. La réaction E2 est favorisée par les bases fortes et les groupes partants de qualité. Elle nécessite une géométrie anti-périplanaire (les atomes à éliminer doivent être situés de part et d'autre de la liaison sigma).
Facteurs influençant le type de réaction
Plusieurs facteurs peuvent influencer le type de réaction qui se produira :
- Structure du substrat: La structure de la molécule de départ affecte la stabilité des intermédiaires réactionnels (carbocations) et l'accessibilité des sites réactionnels.
- Nature du réactif: Les réactifs nucléophiles, électrophiles ou basiques favorisent respectivement les réactions de substitution/addition nucléophile, d'addition électrophile et d'élimination.
- Conditions réactionnelles: Le solvant, la température et la concentration des réactifs peuvent influencer la vitesse et le mécanisme de la réaction.
Ce qu'il faut retenir
- Substitution : Remplacement d'un atome ou groupe d'atomes par un autre. SN1 (unimoléculaire, deux étapes) et SN2 (bimoléculaire, une étape avec inversion).
- Addition : Ajout d'atomes à une molécule, brisant une liaison multiple. Addition électrophile (alcènes) et nucléophile (composés carbonylés).
- Élimination : Retrait d'atomes pour former une liaison multiple. E1 (unimoléculaire, deux étapes) et E2 (bimoléculaire, une étape).
- SN1 : Favorisée par carbocations stables (3° > 2°), solvants polaires protiques.
- SN2 : Favorisée par carbones peu encombrés (1° > 2°), nucléophiles forts. Inversion de configuration.
- E1 : Favorisée par carbocations stables (3° > 2°), solvants polaires protiques.
- E2 : Favorisée par bases fortes, géométrie anti-périplanaire.
- Les réactions de substitution, d'addition et d'élimination sont essentielles en chimie organique.
- Le type de réaction dépend de la structure du substrat, du réactif et des conditions réactionnelles.
FAQ
-
Quelle est la différence entre une réaction SN1 et SN2 ?
La principale différence réside dans le mécanisme. SN1 se déroule en deux étapes avec formation d'un carbocation intermédiaire, tandis que SN2 se déroule en une seule étape avec une inversion de configuration. SN1 est favorisée par les carbocations stables (tertiaires) et les solvants polaires protiques, tandis que SN2 est favorisée par les carbones primaires et les nucléophiles forts. -
Quels sont les facteurs qui influencent le choix entre une réaction d'élimination E1 et E2 ?
La force de la base, la structure du substrat et le solvant jouent un rôle important. Une base forte favorise E2, tandis qu'un substrat formant un carbocation stable favorise E1. E2 nécessite une géométrie anti-périplanaire. -
Pourquoi les réactions d'addition électrophile se produisent-elles principalement sur les alcènes et les alcynes ?
Parce que les alcènes et les alcynes possèdent une liaison π riche en électrons, qui est facilement attaquée par un électrophile (espèce déficitaire en électrons).
